Mời những em nằm trong theo đòi dõi bài học kinh nghiệm thời điểm ngày hôm nay với xài đề
Fe(OH)2 + O2 → Fe2O3 + H2O | Fe(OH)2 đi ra Fe2O3
Thầy cô http://trungtamtiengnhat.edu.vn/ van nài ra mắt phương trình 4Fe(OH)2 + O2 → 2Fe2O3 + 4H2O bao gồm ĐK phản xạ, cơ hội triển khai, hiện tượng kỳ lạ phản xạ và một vài bài bác luyện tương quan chung những em gia tăng toàn cỗ kỹ năng và tập luyện kĩ năng thực hiện bài bác luyện về phương trình phản xạ chất hóa học của Sắt. Mời những em theo đòi dõi bài học kinh nghiệm tại đây nhé:
Bạn đang xem: feoh2 ra fe2o3
Phương trình 4Fe(OH)2 + O2 → 2Fe2O3 + 4H2O
1. Phương trình phản xạ hóa học:
4Fe(OH)2 + O2 → 2Fe2O3 + 4H2O
2. Hiện tượng phân biệt phản ứng
– Chất rắn white color xanh rì Fe(OH)2 chuyển dần dần thanh lịch black color của Fe2O3
3. Điều khiếu nại phản ứng
– Nhiệt chừng cao
4. Tính hóa học hoá học
4.1. Tính hóa học hoá học tập của Fe(OH)2
– Có đặc điểm của bazo ko tan.
– Vừa sở hữu tính lão hóa vừa vặn sở hữu tính khử.
Bị sức nóng phân
– Nung Fe(OH)2 trong ĐK không tồn tại ko khí
Fe(OH)2 
– Nung Fe(OH)2 trong ko khí
4Fe(OH)2 + O2 
Tác dụng với axit
– Với axit không tồn tại tính lão hóa như (HCl, H2SO4)
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
Tính khử:
– Với axit HNO3, H2SO4 đặc
3Fe(OH)2 + 10HNO3 loãng → 3Fe(NO3)3 + NO + 8H2O
2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
– Tác dụng với những hóa học lão hóa khác
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
4.2. Tính hóa học hoá học tập của O2
Khi nhập cuộc phản xạ, vẹn toàn tử O đơn giản dễ dàng nhận thêm thắt 2e. Nguyên tử oxi có tính âm năng lượng điện rộng lớn (3,44), chỉ kém cỏi flo (3,98).
Do vậy, oxi là thành phần phi kim sinh hoạt hoá học tập, sở hữu tính oxi hoá mạnh. Trong những hợp ý hóa học (trừ hợp ý hóa học với flo), thành phần oxi sở hữu số oxi hoá là -2.
Oxi thuộc tính với đa số những sắt kẽm kim loại (trừ Au, Pt, …) và những phi kim (trừ halogen). Oxi thuộc tính với khá nhiều hợp ý hóa học vô sinh và cơ học.
Tác dụng với kim loại
Tác dụng với đa số sắt kẽm kim loại (trừ au và Pt), cần phải có to tạo oxit:
Tác dụng với phi kim
Tác dụng với đa số phi kim (trừ halogen), cần phải có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo đòi tỉ trọng 2:1 về số mol:
Xem thêm: darkseid war vietcomic
Tác dụng với hợp ý chất
– Tác dụng với những hóa học sở hữu tính khử:
– Tác dụng với những hóa học hữu cơ:
5. Cách triển khai phản ứng
– Cho Fe(OH)2 phản ứng với oxi
6. Quý Khách sở hữu biết
Cr(OH)2 cũng sở hữu phản xạ tương tự động với oxi
7. Bài luyện liên quan
Ví dụ 1: Trong những hợp ý hóa học, Fe sở hữu số lão hóa là :
A. +2
B. +3
C. +2; +3
D.0; +2; +3.
Hướng dẫn giải
Đáp án : C
Ví dụ 2: Cho chão Fe giá buốt đỏ loét thuộc tính với oxi nhận được oxit Fe kể từ. Công thức của oxit Fe từ:
A. FeO
B. Fe3O4
C. Fe2O3
D. Fe2O3.nH2O
Hướng dẫn giải
Phương trình phản ứng: 3Fe + 2O2 → Fe3O4
Đáp án : B
Ví dụ 3: Sắt thuộc tính với H2O ở sức nóng chừng cao hom 570°C thì đưa đến H2 và thành phầm rắn là
A. FeO.
B. Fe3O4.
C. Fe2O3.
D. Fe(OH)2.
Hướng dẫn giải
Fe thuộc tính H2O ở t° > 570°C sẽ khởi tạo FeO
t° 3O4
Đáp án : A
8. Một số phương trình phản xạ hoá học tập không giống của Sắt (Fe) và hợp ý chất:
Xem thêm: van chem gio
Trên đó là toàn cỗ nội dung về bài bác học
Fe(OH)2 + O2 → Fe2O3 + H2O | Fe(OH)2 đi ra Fe2O3
. Hy vọng được xem là tư liệu hữu ích chung những em hoàn thành xong chất lượng tốt bài bác luyện của tôi.
Đăng bởi: http://trungtamtiengnhat.edu.vn/
Chuyên mục: Tài Liệu Học Tập

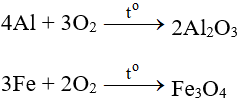
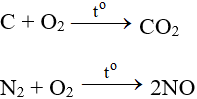
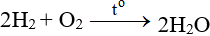
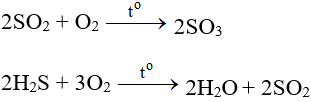










Bình luận